Описание
Препарат Ребиф — современный препарат, обладающий иммуномодулирующими, противовирусными и антипролиферативными свойствами, в основном используется для лечения рассеяного склероза. Основное действующее вещество препарата Ребиф — интерферон бета-1а рекомбинантный человеческий, который представляет собой белковую структуру интерферона бета человека, которую получают методом генной инженерии с использованием культуры клеток яичника китайского хомячка. Препарат Ребиф имеет ту же аминокислотную последовательность, что и эндогенный интерферон бета человека.
Точный механизм действия препарата Ребиф при рассеянном склерозе еще не изучен. Известно, что препарат Ребиф уменьшает частоту и тяжесть клинических рецидивов, способствует ограничению повреждений центральной нервной системы, а соответственно и случаев инвалидизации пациентов с рецидивирующе-ремиттирующим течением рассеянного склероза.
Показания к применению Ребиф
- лечение рассеянного склероза с рецидивирующим течением (т.е. при двух или более обострений заболевания за предшествующие два года)
- Ребиф 44 мкг показан для лечения пациентов, перенесших единичный случай демиелинизирующего заболевания (изолированный синдром) и имеющих риск развития выраженного рассеянного склероза (при исключении других диагнозов).
У пациентов с вторично-прогрессирующим рассеянным склерозом в отсутствии активного течения заболевания эффективность не была продемонстрирована.
Состав Ребиф
1 предварительно заполненный шприц содержит:
- действующее вещество – интерферон бета-1а человеческий рекомбинантный, в дозировке по 22 мкг (6 млн. МЕ) или по 44 мкг (12 млн. МЕ),
- дополнительные вещества: спирт бензиловый,метионин, маннитол, 0.01 М буферный раствор натрия ацетата с рН 4.2, полоксамер 188.
Фармакокинетика
Всасывание и распределение
При подкожном или внутри мышечном введении уровни интерферона бета в сыворотке определяются в течение 12 -24 часов. Независимо от способа введения, препарат Ребиф вызывает значительные фармакодинамические изменения. после внутривенного введения у здоровых добровольцев интерферон бета-1a проявляет резкое мульти-экспоненциальное снижение сывороточных концентраций пропорционально введенной дозировке. Подкожные и внутримышечные введения препарата Ребиф производят эквивалентную экспозицию интерферона-бета.
После однократной инъекции дозы 60 мкг определяемая иммунологическими методами максимальная концентрация, выявляется через три часа и составляет 6-10 ME/мл. При 4-кратной подкожной инъекции одной и той же дозировки каждые 48 часов происходит умеренное накопление вещества. После однократной инъекции внутриклеточная и сывороточная активность 2-5А синтетазы и сывороточная концентрация бета 2 микроглобулина и неоптерина (маркеры биологического ответа) увеличиваются в течение 24 часов, а затем снижаются в пределах 48 часов. Внутримышечное и подкожное введение препарата вызывает одинаковые фармакодинамические изменения.
После повторных подкожных инъекций препарата Ребиф 22 мкг и 44 мкг максимальная концентрация в плазме достигалась в среднем через 8 часов.
Метаболизм и элиминация
Основные фармакокинетические параметры (AUC и Cmax), после введения повторных подкожных инъекций здоровым лицам, увеличивались пропорционально увеличивающейся дозировке с 22 мкг до 44 мкг. Предполагаемый период полураспада составляет от 50 до 60 часов, что соответствует накоплению вещества после приема нескольких дозировок.
Интерферон бета метаболизируется и выводится печенью и почками. Общий клиренс составляет около 33-55 л/час.
Фармакодинамика
При использовании препарата Ребиф в рекомендуемой дозировке выявлено снижение частоты (30 процентов в течение двух лет) и тяжести обострений у пациентов с двумя и более обострениями в течение последних двух лет, и с оценкой степени инвалидизации (EDSS) перед началом лечения от 0 до 5 по расширенной шкале оценки. Доля пациентов с подтвержденным прогрессированием инвалидизации уменьшилась с 39 процентов (плацебо) до 30процентов и 27процентов (Ребиф 22 мкг и 44 мкг соответственно).
Через четыре года среднее снижение числа обострений составляло 22 процента и 29 процентов у пациентов, получавших Ребиф 22 мкг и Ребиф 44 мкг соответственно по сравнению с группой пациентов, получавших плацебо два года , а затем Ребиф 22 мкг и Ребиф 44 мкг.
В 3-летнем исследовании у пациентов с вторично-прогрессирующим рассеянным склерозом (3-6.5 по шкале EDSS) с достоверным прогрессированием инвалидизации в течение предшествующих 2 лет и отсутствием обострений в течение предшествующих восьми недель, препарат Ребиф не проявлял значительного влияния на инвалидизацию, тем не менее частота обострений понизилась на 30 процентов. При распределении на две группы пациентов (с и без обострений в течение предшествующих 2 лет): в группе «без обострений» не было обнаружено влияние лекартства на прогрессирование инвалидизации, тогда как в группе больных с «обострениями» доля с прогрессированием в конце эксперимента понизилась с 70 процентов (плацебо) до 57 процентов (Ребиф 22 мкг и Ребиф 44 мкг).
Действие Ребифа не изучалось при первично-прогрессирующем рассеянном склерозе.
Если терапия пациентов начиналась с введения препарата Ребиф 44 мкг, то на протяжении 8-летнего курса лечения наблюдалось замедление прогрессирования заболевания (согласно индексам расширенной шкалы оценки инвалидизации — EDSS), снижение частоты развития рецидивов и величины поражения по данным МРТ, по сравнению с результатами, полученными при лечении больных на протяжении двух лет плацебо, а затем – препаратом Ребиф.
Согласно этим данным, считается, что при раннем начале лечения пациентов с рецидивирующе-ремиттирующим течением рассеянного склероза можно добиться стойкого положительного результата по сравнению с пациентами, у которых лечение прерывалось. Этот эффект более выражен при применении высших доз препарата.
Ввиду того, что у больных с первично-прогрессирующим течением рассеянного склероза эффективность препарата не изучалась, Ребиф не следует применять для лечения этой категории пациентов.
У пациентов, испытавших единичный клинический случай, напоминающий демиелинизацию по причине рассеянного склероза, также были проведены клинические исследования препарата Ребиф. Пациенты были распределены по принципу двойного слепого исследования на группы, в которых Ребиф 44 мкг вводили 3 раза в неделю и Ребиф 44 мкг – один раз в неделю или плацебо.
При проявлении второго клинического случая демиелинизации, подтверждающего достоверный рассеянный склероз, пациенты были переведены на рекомендованную дозировку препарата Ребиф 44 мкг по три раза в неделю.
Доклиническая безопасность
Какую-либо опасность для человека доклинические данные не выявили. Исследование проводилось, основываясь на традиционных исследованиях безопасности фармакологии, токсичности повторных доз и генотоксичности. Канцерогенность Ребифа не изучалась. Каких-либо нарушений токсичности у эмбриона/плода обезьян исследование не показало. Основываясь на данных по другим альфа и бета интерферонам, повышенный риск выкидышей не может быть исключен.
Применение при нарушениях функции печени
пациентам с тяжелой печеночной недостаточностью следует назначать препарат с осторожностью и под строгим контролем врача.
Применение при нарушениях функции почек
Пациентам с тяжелой почечной недостаточностью следует назначать препарат с осторожностью и под строгим контролем врача.
Применение у детей
Противопоказан в детском возрасте до 12 лет.
Как правило, подросткам в возрасте от 12 лет до 16 лет препарат назначают в дозировка по 22 мкг три раза в неделю.
Фармацевтические характеристики Ребиф
Бесцветный или светло-желтый прозрачный или слегка опалесцирующий раствор.
Упаковка, срок годности, условия хранения
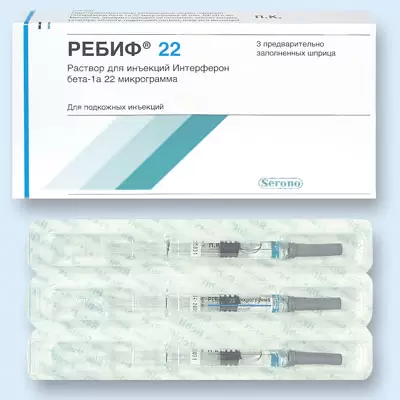
- По 0.5 мл препарата (с дозировкой по 22 мкг и по 44 мкг) помещены в бесцветные стеклянные шприцы c пробкой-поршнем, иглой и с двойным защитным колпачком колпачком. Предварительно заполненный шприц размещают в контурную ячейковую упаковку из ПВХ с верхним бумажным покрытием. По 3 или 12 контурных упаковок вместе с инструкцией по применению упакованы в коробку картонную.
- По 1,5 мл препарата (3 дозы) размещены в картриджи из прозрачного бесцветного боросиликатного стекла номинальной вместимостью 3 мл, укупоренные силиконизированным резиновым шток-поршнем, алюминиевым колпачком с резиновой прокладкой. По одному картриджу упакованы в пластиковый контейнер и запечатаны прозрачной пленкой. По 4 пластиковых контейнера помещают в картонную пачку.
Хранить при температуре 2°С – 8°С (в холодильнике) в оригинальной упаковке. Не замораживать. Хранить в недоступном для детей месте!
Транспортировать при температуре от 2° до 8°C.
Срок хранения 2 года
Не применять после окончания срока годности, указанного на упаковке.
Наша компания работает как на территории Кыргызстана, так и осуществляет доставку в страны ближнего зарубежья. Обращайтесь к нам за консультациями по контактным телефонам.
Заказать и купить Ребиф (интерферон бета-1а) в Бишкек
Заказать и купить Ребиф (интерферон бета-1а) в Кыргызстане
Позвоните и узнайте цену Ребиф (интерферон бета-1а)
Работаем и отправляем Ребиф (интерферон бета-1а) по странам СНГ: Казахстан (Алматы и Нур-Султан), Россия, Украина, Белоруссия, Узбекистан (Ташкент),
а также можем отправить Ребиф (интерферон бета-1а) по регионам Кыргызстана: Ош, Джалал-Абад, Каракол, Узген, Балыкчы и другие.



Отзывы
Отзывов пока нет.